 同社は、1980年から非臨床試験業務のコンピューター化への取り組みを開始し、1992年からパッケージソフト「LATOX-F」を提供してきていた。今回の「tsPharma LabSite」は、長年培った経験と実績を生かすとともに、武田薬品工業と第一三共の開発協力を得て、試験実施手順などの現場のノウハウと実際に利用している独自開発のシステム資産をフルに利用。将来的なニーズにも柔軟に対応できる最新パッケージとして、機能の充実を図ったという。
同社は、1980年から非臨床試験業務のコンピューター化への取り組みを開始し、1992年からパッケージソフト「LATOX-F」を提供してきていた。今回の「tsPharma LabSite」は、長年培った経験と実績を生かすとともに、武田薬品工業と第一三共の開発協力を得て、試験実施手順などの現場のノウハウと実際に利用している独自開発のシステム資産をフルに利用。将来的なニーズにも柔軟に対応できる最新パッケージとして、機能の充実を図ったという。
富士通が新しい非臨床安全性試験パッケージを製品化
大手製薬会社が開発協力、規制の変化などにも柔軟対応
2014.09.26−富士通は25日、製薬業界やCRO(医薬品開発受託機関)向けの新しい非臨床安全性試験パッケージ「FUJITSU Life Science Solution tsPharma LabSite」を開発、販売開始したと発表した。GLP(医薬品の安全性に関する非臨床試験の実施基準)試験のアウトソーシング化の拡大や使用動物数を減らした試験内容への変更の増加、さらに日米EU医薬品規制調和国際会議(ICH)の動向、規制要件変更や今後の電子化申請への対応など、製薬業を取り巻く新しい情勢の変化に柔軟に対応できるように開発されたもの。クライアント/サーバー型のシステムで、価格は最小構成で1,450万円から。3年間で25社への販売を見込んでいる。
 同社は、1980年から非臨床試験業務のコンピューター化への取り組みを開始し、1992年からパッケージソフト「LATOX-F」を提供してきていた。今回の「tsPharma LabSite」は、長年培った経験と実績を生かすとともに、武田薬品工業と第一三共の開発協力を得て、試験実施手順などの現場のノウハウと実際に利用している独自開発のシステム資産をフルに利用。将来的なニーズにも柔軟に対応できる最新パッケージとして、機能の充実を図ったという。
同社は、1980年から非臨床試験業務のコンピューター化への取り組みを開始し、1992年からパッケージソフト「LATOX-F」を提供してきていた。今回の「tsPharma LabSite」は、長年培った経験と実績を生かすとともに、武田薬品工業と第一三共の開発協力を得て、試験実施手順などの現場のノウハウと実際に利用している独自開発のシステム資産をフルに利用。将来的なニーズにも柔軟に対応できる最新パッケージとして、機能の充実を図ったという。
特徴的な機能としては、GLP適用試験に対応していることに加え、米食品医薬品局(FDA)が定めた電子データと電子署名に関する規則である21CFRパート11に準拠。実際に試験時に使用される400種類以上の帳票レイアウトを標準テンプレートとして提供することが可能で、今後予定されている申請電子データの標準である“CDISC SEND”にも対応している。
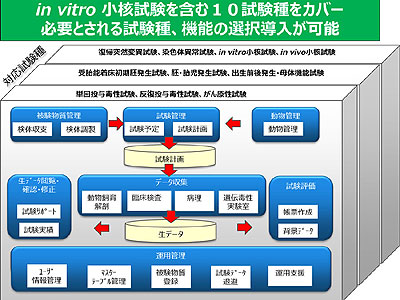
また、新たにICH S2(R1)ガイドラインで採用されたin vitro小核試験を含むICH M3(R2)ガイドラインで規定された10種類の試験種と、試験データ検索やスケジュール管理などの11種類のオプション機能、およびクライアントライセンス数をそれぞれ組み合わせて最適な構成で利用することが可能。GLP適用試験の通常の測定項目にない任意の測定を追加するなど、GLP非適用・非定型な試験計画にも対応するほか、毒性試験機能を用いた局所刺激性試験、in vivo光毒性試験の実施など適用範囲を広げることもできる。
******
<関連リンク>:
富士通(ライフサイエンスソリューションのトップページ)
http://jp.fujitsu.com/solutions/life/
富士通(tsPharma 紹介ページ)
http://jp.fujitsu.com/solutions/life/concept/tspharma/